Sinopharm (Пекін): BBIBP-CorV
ФАЗА 1
1 Судовы працэс
ChiCTR2000032459
Кітай
ФАЗА 2
2 выпрабаванні
NCT04962906
Аргенціна
ChiCTR2000032459
Кітай
ФАЗА 3
6 выпрабаванняў
NCT04984408
ChiCTR2000034780
Абяднаныя Арабскія Эміраты
NCT04612972
Перу
NCT04510207
Бахрэйн, Егіпет, Іарданія, Аб'яднаныя Арабскія Эміраты
NCT04560881, BIBP2020003AR
Аргенціна
NCT04917523
Абяднаныя Арабскія Эміраты
Ухвалы
Спіс СААЗ па надзвычайных сітуацыях 59 краін
Ангола, Аргенціна, Бахрэйн, Бангладэш, Беларусь, Беліз, Балівія (шматнацыянальная дзяржава), Бразілія, Бруней -Даруссалам, Камбоджа, Камерун, Чад, Кітай, Каморскія астравы, Егіпет, Экватарыяльная Гвінея, Габон, Гамбія, Грузія, Грузія 、 Іран (Ісламская Рэспубліка) 、 Ірак 、 Іарданія 、 Кыргызстан 、 Лаоская Народна -Дэмакратычная Рэспубліка
Ліван, Малайзія, Мальдывы, Маўрытанія, Аўрыкій, Манголія, Чарнагорыя, Марока, Мазамбік, Намібія, Непал, Нігер, Паўночная Македонія, Пакістан, Парагвай, Перу, Філіпіны, Рэспубліка Конга, Энегал, Сербія, Сейр Астравы, Самалі, Шры -Ланка, Тайланд, Трынідад і Табага, Туніс, Аб'яднаныя Арабскія Эміраты, Венесуэла (Баліварыянская Рэспубліка), В'етнам, Зімбабвэ
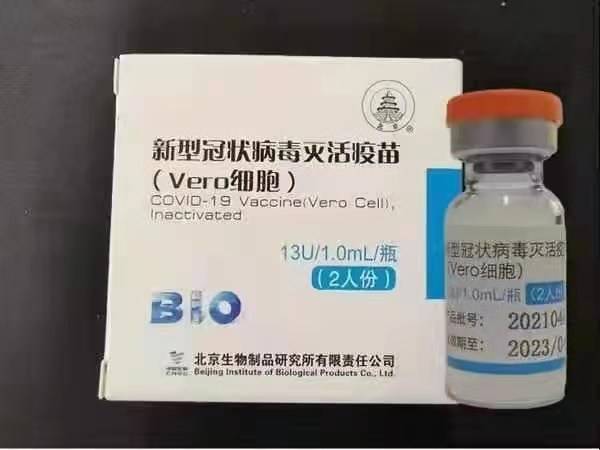
Sinopharm BBIBP-CorV COVID-19-гэта інактываваная вакцына, вырабленая з культурна вырашчаных вірусных часціц, якія не валодаюць патагеннымі здольнасцямі. Гэты кандыдат на вакцыну быў распрацаваны кампаніяй Sinopharm Holdings і Пекінскім інстытутам біялагічных прадуктаў.
Вакцына Sinopharm BBIBP-CorV дзейнічае, дазваляючы імуннай сістэме выпрацоўваць антыцелы супраць бэта-коронавіруса SARS-CoV-2. Інактываваныя вакцыны супраць вірусаў выкарыстоўваюцца на працягу многіх дзесяцігоддзяў, напрыклад, вакцына супраць шаленства і вакцына супраць гепатыту А. Гэтая тэхналогія распрацоўкі паспяхова ўжываецца ў многіх вядомых вакцынах, напрыклад вакцыне супраць шаленства.
Штам SARS-CoV-2 Sinopharm (штам WIV04 і бібліятэчны нумар MN996528) быў выдзелены ад пацыента ў бальніцы Цзіньінтань у горадзе Ухань, Кітай. Вірус быў размножаны ў культуры ў кампетэнтнай клетачнай лініі Vero, і супернатант інфікаваных клетак інактывавалі β-пропіёлактонам (1: 4000 аб./Аб., Ад 2 да 8 ° C) на працягу 48 гадзін. Пасля ўдакладнення клеткавага смецця і ультрафільтрацыі была праведзена другая інактывацыя β-пропиолактона пры тых жа ўмовах, што і першая інактывацыя. Па дадзеных СААЗ, вакцыну адсарбавалі на 0,5 мг галыну і загрузілі ў папярэдне запоўненыя шпрыцы ў 0,5 мл стэрыльнага солевага раствора з буферам з фасфатамі без кансервантаў.
31 снежня 2020 года Дзяржаўная адміністрацыя лекаў абвясціла аб зацвярджэнні эксперыментальнай вакцыны, распрацаванай Sinopharm.
7 мая 2021 года Сусветная арганізацыя аховы здароўя абвясціла аб ухваленні вакцыны. Спіс СААЗ па надзвычайных сітуацыях дазволіў краінам паскорыць уласныя нарматыўныя дакументы на імпарт і ўвядзенне вакцыны супраць COVID-19. Кансультатыўная група экспертаў СААЗ па стратэгіях імунізацыі таксама завяршыла агляд вакцыны. Зыходзячы з усіх наяўных дадзеных, СААЗ рэкамендуе дзве дозы вакцыны з інтэрвалам у тры -чатыры тыдні для дарослых ад 18 гадоў. Эфектыўнасць вакцыны супраць сімптаматычнага і шпіталізаванага захворвання ацэньваецца ў 79% для ўсіх узроставых груп разам узятых.
Амерыканская медыцынская асацыяцыя апублікавала "рандомізаванае клінічнае выпрабаванне: уплыў 2 інактываваных вакцын супраць SARS-CoV-2 на сімптаматычную інфекцыю COVID-19 у дарослых" 26 мая 2021 года, прыйшоўшы да высновы, што "ў гэтым папярэдне вызначаным прамежкавым аналізе рандомізіраванага клінічнага выпрабавання, дарослыя 2 інактываваныя вакцыны супраць SARS-CoV-2, уведзеныя ў гэтым загадзя вызначаным прамежкавым аналізе рандомізіраваных клінічных выпрабаванняў, значна знізілі рызыку сімптаматычнага COVID-19, а сур'ёзныя пабочныя дзеянні былі рэдкімі ". У гэтым рандомізіраваным даследаванні 3 фазы на дарослых эфектыўнасць 2 інактываваных вакцын з цэлым вірусам у сімптаматычных выпадках COVID-19 склала 72,8% і 78,1% адпаведна. 2 вакцыны мелі рэдкія сур'ёзныя пабочныя дзеянні з аналагічнай частатой, чым група кіравання толькі квасцом, і большасць з іх не мела дачынення да вакцынацыі. Даследчы аналіз выявіў, што 2 вакцыны выклікалі вымяральныя нейтралізуючыя антыцелы, аналагічныя вынікам выпрабаванняў фазы 1/2.
Рабочая група САЗЕ СААЗ апублікавала агляд вакцыны Sinopharm/BBIBP супраць COVID-19 10 мая 2021 года. Вакцына GAVI супраць COVID-19 уключае манітор з флакона вакцыны, які паведамляе медыцынскім работнікам, ці правільна захоўвалася вакцына і ці не падвяргалася ўздзеянню. перагрэў. У выніку 14 мая 2021 г. GAVI паведаміла пра пашкоджанні. Разумныя этыкеткі вытворчасці Zebra Technologies і вытворчасці Temptime Corporation складаюцца з круга з больш светлым каляровым квадратам пасярэдзіне, зробленага з бясколернага хімічнага рэчыва, якое з цягам часу незваротна фармуе колер . Гэта становіцца больш цёмным, каб даць візуальную прыкмету сукупнага цеплавога ўздзеяння. Пасля таго, як флакон быў падвергнуты ўздзеянню цяпла за межамі яго аптымальнага дыяпазону захоўвання, квадрат становіцца больш цёмным, чым круг, што паказвае на тое, што вакцыну выкарыстоўваць больш нельга.
Рэгістрацыйны нумар Нацыянальнай бібліятэкі лекаў супраць вакцыны супраць COVID-19 супраць лекавых прэпаратаў BBIBP-CorV: DB15807.